新潟市医師会報より

冠動脈疾患におけるこれからの至適抗血栓療法を考える~Aspirin-free strategy~
新潟市民病院 循環器内科副部長 土田 圭一
はじめに
アセチルサリチル酸(以下アスピリン)は今から120年前に消炎鎮痛剤として商品化され、50年前にはじめて抗血栓作用の機序が解明されて以来、心血管病の1次・2次予防治療薬として不可欠な薬剤と位置付けられてきた。しかし近年、新たな抗血栓薬が次々と開発され、またスタチンや新規の糖尿病治療薬の優れた2次予防効果を示す研究結果が多く示されるようになり、アスピリンの心血管病予防効果の有効性について疑問が呈されるようになっている。本稿では、これまでのアスピリンの心血管病予防効果についてのエビデンスを紹介し、その上で最近の冠動脈疾患、ことに経皮的冠動脈インターベンション(PCI)後の至適抗血栓療法のあり方についての変遷と今後の見通しについて文献的考察を交えて述べたいと思う。
これまでのアスピリンのエビデンス
過去30年間にアスピリンについては多くの心血管病1次予防に関する臨床試験が行われてきたが、実際に真に有効性を示した研究は少なく、2000年代初頭に行われたAntithrombotic Trialists’ Collaboration(ATT)メタ解析では死亡率の低下は示せなかった1)。多くの試験では出血事故の増加により便益が相殺されるか、不利益が便益に勝る結果となってきた。アスピリンの有効性については古典的な論争があり、胃腸障害の副作用の他、アスピリンジレンマ(アスピリンの投与量により血栓形成抑制効果が減弱されたり増強されたりする現象)や、アスピリン抵抗性(血小板機能が予期した通りには抑制されない場合があること)などが、不確実な抗血栓作用の要因として考えられている。ATTメタ解析結果は、1970年代の患者データを基に行われた臨床試験も含まれており、2000年代に入りあらためてアスピリンの1次予防を検討するため、ARRIVE2)、ASCEND3)、ASPREE4)の3つの臨床試験が行われたが、1次予防効果を示したのは糖尿病患者を対象としたASCENDのみで、いずれの試験においても重大出血がアスピリン群で有意に増加する結果となり、最新のエビデンスとしてもアスピリンの1次予防における有効性を示すデータは乏しいといえる。
一方で、アスピリンは心血管イベント2次予防において、依然としてクラスⅠ、エビデンスレベルAで使用することが本邦ならびに欧米のガイドラインにて推奨されている(表1)5)−7)。しかし長年議論の余地がないところであったアスピリンの2次予防効果についても、近年その基盤薬としての安全性と有効性に対して再考がなされている。その主な論拠としては、アスピリンによる重大出血リスクへの懸念のほか、近年のスタチンや降圧薬、新規糖尿病治療薬によるリスクファクター管理による2次予防効果や新規抗血栓薬(P2Y12受容体拮抗薬、直接型経口抗凝固薬)の登場によるアスピリンの2予防薬としての地位の相対的低下があるとする見解である8)。アスピリンの心血管イベント2次予防に関する臨床試験は、1989年のTASS研究9)にはじまり、現在に至るまでの約30年間に急性冠症候群(ACS)や心筋梗塞既往歴を有する患者、およびPCI施行例を対象として数多く行われてきたが、2013年以降、アスピリンを含まない抗血栓療法のレジメンがPCI後の冠動脈疾患患者を対象に、その安全性と有効性が検討されるようになった。このようなaspirin-free strategyが生まれてきた背景としては、上述のような論拠のほか、PCIで使用される冠動脈ステントの革新的な改良も要因の1つとすることができる。
PCI後の抗血栓療法:出血リスク重視へのシフト
2004年に本邦で臨床使用が開始された薬剤溶出性ステント(drug-eluting stent; DES)により、従来のメタルステントの課題であった再狭窄を撲滅する可能性が示されるようになった10)。しかし第1世代DESではステント留置部の内皮化の著しい遅延や、生体適合性の不良なポリマーの残存による炎症反応の持続によるステント血栓症のリスクが長期に持続するという懸念から11)、12)、ステント留置後に必須であるアスピリンとP2Y12受容体拮抗薬の2剤併用療法(dual antiplatelet therapy; DAPT)は最低12ヶ月間継続することが標準治療とされてきた。2010年代以降に導入された第2世代DESでは、ステント留置部の治癒安定化の促進がはかられ、第1世代DESに比べ明らかにステント血栓症の頻度が低いことが明らかとなった13)、14)。第2世代以後のDESを用いた至適DAPT期間を検証した多くの臨床試験により、1年以上の長期DAPTの有効性を証明する結果は得られず、むしろ重大出血による死亡率の上昇を示す報告15)が散見されるようになり、DAPT期間は短縮化へ舵が切られるようになり、より短期間のDAPT期間の安全性・有効性の検証が進むこととなった。2010年から2018年の間に報告された18の臨床研究を基にしたメタ解析では、短期DAPT(<6ヶ月)は長期DAPT(≧12ヶ月)に比べ有意に重大出血や非心臓死が少なく、標準DAPT(12ヶ月)との比較でもあらゆる出血事象が少なかった。特に第2世代以降のDESに限ると長期DAPTは短期DAPTに比べ有意に全死亡も増えるという結果であった16)。一方で心筋梗塞やステント血栓症などのイベント予防効果においては、短期DAPTと標準DAPTでは差はないものの、長期DAPTにおいて有意に抑制効果が優れていた16)。
以上のような背景から、第1世代DES時代で行われていたような一律にDAPT期間を設定するやり方から、DAPT期間を患者ごとの出血リスク・血栓リスクから個別化して判断するアプローチが提唱され、出血リスクスコアが考案された。当初米国と欧州でそれぞれDAPT score17)、PRECISE DAPT score18)という異なるツールが用いられていたが、その後欧米の医師、研究者が学術研究協議会(Academic Research Consortium; ARC)を組織し、新たにHBR(High Bleeding Risk)基準を考案した19)。年齢、肝腎機能障害、悪性腫瘍罹患、貧血の有無など合計12項目からHBRにあたるか否かを個別に検討し、DAPT期間決定に役立てようという訳である。ARC HBRは有用なツールであるが、抗血栓療法に対するtherapeutic windowが白人にくらべ出血リスクにシフトする傾向のある東アジア人種において、はたして普遍化できるかという問題があり20)、その後本邦でもARC HBR基準を参考に、主要項目として腎機能障害、貧血のほか低体重、心不全、末梢動脈疾患を加えた5項目と、9つの副項目からなる日本版HBR基準が考案された21)。
心房細動の合併例はPCIを考慮される患者の中でも、特に出血リスクの高いグループである。すなわち抗凝固薬に加え、冠動脈ステント留置後にDAPTが加わり、いわゆる3剤併用療法(triple therapy)となるからであるが、この患者群の至適抗血栓薬のあり方を明らかにしたのがWOEST試験である22)。この試験ではtriple therapyとアスピリンを含まないワルファリン+P2Y12拮抗薬(クロピドグレル)の2剤療法とを比較し、重大出血イベントは2剤で有意に低かっただけでなく、虚血性イベントも2剤の方が有意に低かったという結果となった22)。この研究以降、非心房細動例で抗凝固薬が不要な患者においても、DAPT期間の短縮に加えて、抗血小板薬単剤へde-escalationする際にアスピリンを中止するaspirin-free strategyの妥当性が数多く示されることとなる。
PCI後の抗血栓療法:Aspirin-free strategyの妥当性と展望
aspirin-free strategyへの萌芽は、実はWOEST試験よりも以前の1990年代に行われたCAPRIE研究にみることができる23)。虚血性脳卒中、心筋梗塞、末梢動脈疾患患者の2次予防のためP2Y12拮抗薬であるクロピドグレル75mgと高用量(325mg)のアスピリンを比較した試験であったが、アスピリンに比べクロピドグレルで約9%心血管イベントを抑制したという結果であった23)。アスピリンの冠動脈疾患の2次予防効果については、前出のATTメタ解析結果でも有効性が示されているが、実際にはPCI後の患者は多くは含まれておらず、データが不足していた1)。その後、より新世代のP2Y12拮抗薬としてプラスグレル、チカグレロルの2剤が登場し(表2)24)、主にACS患者を対象に、クロピドグレルとの比較研究が行われ、心血管イベント抑制効果は新世代の2剤において優れている一方で、出血リスクはクロピドグレルで低率といった結果であった。冠動脈疾患2次予防におけるこれらP2Y12拮抗薬のエビデンスの集積を受けてPCI後のaspirin-free strategyを検証する重要な臨床試験の結果が2018年以降複数発表された。GLOBAL LEADERS試験では、チカグレロルとアスピリンによるDAPT期間1ヵ月の後にアスピリンを中止しチカグレロルを継続する群と、チカグレロルまたはクロピドグレル+アスピリンによるDAPT期間12ヵ月の後にアスピリンを継続する群を比較検討した。DAPT期間1ヵ月群の心筋梗塞および全死亡の減少は示されなかったが、post hoc解析であるがACS 患者において、1ヶ月群で虚血イベントを増加させることなく出血イベントの減少が認められた。TWILIGHT試験は、65%をACSが占める患者を対象としチカグレロル+アスピリンのDAPTを3ヵ月継続後アスピリンを中止する群と、DAPTを継続する群を比較し、アスピリン中止群で出血イベントは有意に少なく、虚血イベントの発生率は同等であった。本邦で行われたSTOPDAPT-2試験には安定冠動脈疾患患者が多く含まれていたが、DAPT継続期間1ヵ月の後にクロピドグレルを継続する群とDAPTを12ヶ月継続する群を比較検討したところ、DAPT継続期間1ヵ月群において、死亡、心筋梗塞、脳卒中、ステント血栓症、出血(TIMI出血基準の大出血・小出血)から評価したネットクリニカルベネフィット(リスクを考慮した上での総合的な有用性)が良好であることが示された。以上からDAPT継続終了後に、アスピリンよりも強い抗血小板作用を有すると考えられるP2Y12受容体拮抗薬を継続する処方を高リスク患者で考慮することは妥当であると考えられ、DAPT期間はついに1ヶ月でも可能とする時代となった。一方でACS患者のみを対象にした1ヶ月DAPT後にクロピドグレル単剤とする群とDAPTを継続する群を比較したSTOPDAPT-2ACS試験では、有意差はなかったものの心血管イベントが1ヶ月DAPT群で上昇する傾向を示す結果となった25)。最新の本邦のガイドラインでは、前述の日本版HBR基準、抗凝固薬の服用の有無、ACSなどの血栓リスクに基づいてDAPT期間を決定し、DAPT期間終了後の単剤療法はアスピリン、P2Y12拮抗薬いずれでもよいとされている(図)。今後は上述のエビデンスを踏まえSAPT時のaspirin-freeが明記される可能性がある。
今まで述べてきたように常に投与が基本とされてきたアスピリンの有効性・安全性のエビデンスレベルは近年低下し、効果が確実で早いP2Y12受容体拮抗薬の普及もあり、aspirin-free strategyへのシフトはさらに進むものと予想される。一方でアスピリンを中止することによるコストベネフィットや潜在的な癌予防・認知機能改善効果などの心血管系以外の多面的な好ましい効果の喪失なども秤にかけ考えるべきかもしれない26)。
最後に
冠動脈疾患、特にPCI後の最新の抗血栓療法のあり方について概説してきた。アスピリンの2次予防効果は十分認識されるべきであるが、そのエビデンスは近年の実地臨床からは一昔前の研究から得られたものであり再考されるべき時期に来ている。第2世代以降のDESの優れた抗血栓性と、PCI後の出血イベントの生命に与える影響からPCI後のDAPT期間はより短縮され、またアスピリンを含まない抗血栓薬治療の妥当性が多くの試験で証明されている。PCIが今後さらに安全で確実な低侵襲治療へ発展するために、これからも最新の知見を踏まえた最適な抗血栓療法のあり方は今後ともアップデートがなされていくものと予想される。
参考文献
1)Antithrombotic Trialists C, Baigent C, Blackwell L, Collins R, Emberson J, Godwin J, Peto R, Buring J, Hennekens C, Kearney P, Meade T, Patrono C, Roncaglioni MC and Zanchetti A. Aspirin in the primary and secondary prevention of vascular disease: collaborative meta-analysis of individual participant data from randomised trials. Lancet. 2009; 373: 1849-60.
2)Gaziano JM, Brotons C, Coppolecchia R, Cricelli C, Darius H, Gorelick PB, Howard G, Pearson TA, Rothwell PM, Ruilope LM, Tendera M, Tognoni G and Committee AE. Use of aspirin to reduce risk of initial vascular events in patients at moderate risk of cardiovascular disease (ARRIVE): a randomised, double-blind, placebo-controlled trial. Lancet. 2018; 392: 1036-1046.
3)Group ASC, Bowman L, Mafham M, Wallendszus K, Stevens W, Buck G, Barton J, Murphy K, Aung T, Haynes R, Cox J, Murawska A, Young A, Lay M, Chen F, Sammons E, Waters E, Adler A, Bodansky J, Farmer A, McPherson R, Neil A, Simpson D, Peto R, Baigent C, Collins R, Parish S and Armitage J. Effects of Aspirin for Primary Prevention in Persons with Diabetes Mellitus. N Engl J Med. 2018; 379: 1529-1539.
4)McNeil JJ, Wolfe R, Woods RL, Tonkin AM, Donnan GA, Nelson MR, Reid CM, Lockery JE, Kirpach B, Storey E, Shah RC, Williamson JD, Margolis KL, Ernst ME, Abhayaratna WP, Stocks N, Fitzgerald SM, Orchard SG, Trevaks RE, Beilin LJ, Johnston CI, Ryan J, Radziszewska B, Jelinek M, Malik M, Eaton CB, Brauer D, Cloud G, Wood EM, Mahady SE, Satterfield S, Grimm R, Murray AM and Group AI. Effect of Aspirin on Cardiovascular Events and Bleeding in the Healthy Elderly. N Engl J Med. 2018; 379: 1509-1518.
5)日本循環器学会 急性冠症候群ガイドライン2018年.
6)Visseren FLJ, Mach F, Smulders YM, Carballo D, Koskinas KC, Back M, Benetos A, Biffi A, Boavida JM, Capodanno D, Cosyns B, Crawford C, Davos CH, Desormais I, Di Angelantonio E, Franco OH, Halvorsen S, Hobbs FDR, Hollander M, Jankowska EA, Michal M, Sacco S, Sattar N, Tokgozoglu L, Tonstad S, Tsioufis KP, van Dis I, van Gelder IC, Wanner C, Williams B and Group ESCSD. 2021 ESC Guidelines on cardiovascular disease prevention in clinical practice. Eur J Prev Cardiol. 2021.
7)Smith SC, Jr., Benjamin EJ, Bonow RO, Braun LT, Creager MA, Franklin BA, Gibbons RJ, Grundy SM, Hiratzka LF, Jones DW, Lloyd-Jones DM, Minissian M, Mosca L, Peterson ED, Sacco RL, Spertus J, Stein JH and Taubert KA. AHA/ACCF secondary prevention and risk reduction therapy for patients with coronary and other atherosclerotic vascular disease: 2011 update: a guideline from the American Heart Association and American College of Cardiology Foundation endorsed by the World Heart Federation and the Preventive Cardiovascular Nurses Association. J Am Coll Cardiol. 2011; 58: 2432-46.
8)Capodanno D, Mehran R, Valgimigli M, Baber U, Windecker S, Vranckx P, Dangas G, Rollini F, Kimura T, Collet JP, Gibson CM, Steg PG, Lopes RD, Gwon HC, Storey RF, Franchi F, Bhatt DL, Serruys PW and Angiolillo DJ. Aspirin-free strategies in cardiovascular disease and cardioembolic stroke prevention. Nat Rev Cardiol. 2018; 15: 480-496.
9)Hass WK, Easton JD, Adams HP, Jr., Pryse-Phillips W, Molony BA, Anderson S and Kamm B. A randomized trial comparing ticlopidine hydrochloride with aspirin for the prevention of stroke in high-risk patients. Ticlopidine Aspirin Stroke Study Group. N Engl J Med. 1989; 321: 501-7.
10)Morice MC, Serruys PW, Sousa JE, Fajadet J, Ban Hayashi E, Perin M, Colombo A, Schuler G, Barragan P, Guagliumi G, Molnar F, Falotico R and Lesions RSGRSwtS-CBVB-ESitToPwdNNCA. A randomized comparison of a sirolimus-eluting stent with a standard stent for coronary revascularization. N Engl J Med. 2002; 346: 1773-80.
11)Daemen J, Wenaweser P, Tsuchida K, Abrecht L, Vaina S, Morger C, Kukreja N, Juni P, Sianos G, Hellige G, van Domburg RT, Hess OM, Boersma E, Meier B, Windecker S and Serruys PW. Early and late coronary stent thrombosis of sirolimus-eluting and paclitaxel-eluting stents in routine clinical practice: data from a large two-institutional cohort study. Lancet. 2007; 369: 667-78.
12)Finn AV, Kolodgie FD, Harnek J, Guerrero LJ, Acampado E, Tefera K, Skorija K, Weber DK, Gold HK and Virmani R. Differential response of delayed healing and persistent inflammation at sites of overlapping sirolimus- or paclitaxel-eluting stents. Circulation. 2005; 112: 270-8.
13)Otsuka F, Vorpahl M, Nakano M, Foerst J, Newell JB, Sakakura K, Kutys R, Ladich E, Finn AV, Kolodgie FD and Virmani R. Pathology of second-generation everolimus-eluting stents versus first-generation sirolimus- and paclitaxel-eluting stents in humans. Circulation. 2014; 129: 211-23.
14)Sabate M, Brugaletta S, Cequier A, Iniguez A, Serra A, Hernadez-Antolin R, Mainar V, Valgimigli M, Tespili M, den Heijer P, Bethencourt A, Vazquez N, Backx B and Serruys PW. The EXAMINATION trial (Everolimus-Eluting Stents Versus Bare-Metal Stents in ST-Segment Elevation Myocardial Infarction): 2-year results from a multicenter randomized controlled trial. JACC Cardiovasc Interv. 2014; 7: 64-71.
15)Valgimigli M, Campo G, Monti M, Vranckx P, Percoco G, Tumscitz C, Castriota F, Colombo F, Tebaldi M, Fuca G, Kubbajeh M, Cangiano E, Minarelli M, Scalone A, Cavazza C, Frangione A, Borghesi M, Marchesini J, Parrinello G, Ferrari R and Prolonging Dual Antiplatelet Treatment After Grading Stent-Induced Intimal Hyperplasia Study I. Short- versus long-term duration of dual-antiplatelet therapy after coronary stenting: a randomized multicenter trial. Circulation. 2012; 125: 2015-26.
16)Yin SH, Xu P, Wang B, Lu Y, Wu QY, Zhou ML, Wu JR, Cai JJ, Sun X and Yuan H. Duration of dual antiplatelet therapy after percutaneous coronary intervention with drug-eluting stent: systematic review and network meta-analysis. BMJ. 2019; 365: l2222.
17)Yeh RW, Secemsky EA, Kereiakes DJ, Normand SL, Gershlick AH, Cohen DJ, Spertus JA, Steg PG, Cutlip DE, Rinaldi MJ, Camenzind E, Wijns W, Apruzzese PK, Song Y, Massaro JM, Mauri L and Investigators DS. Development and Validation of a Prediction Rule for Benefit and Harm of Dual Antiplatelet Therapy Beyond 1 Year After Percutaneous Coronary Intervention. JAMA. 2016; 315: 1735-49.
18)Costa F, van Klaveren D, James S, Heg D, Raber L, Feres F, Pilgrim T, Hong MK, Kim HS, Colombo A, Steg PG, Zanchin T, Palmerini T, Wallentin L, Bhatt DL, Stone GW, Windecker S, Steyerberg EW, Valgimigli M and Investigators P-DS. Derivation and validation of the predicting bleeding complications in patients undergoing stent implantation and subsequent dual antiplatelet therapy (PRECISE-DAPT) score: a pooled analysis of individual-patient datasets from clinical trials. Lancet. 2017; 389: 1025-1034.
19)Urban P, Mehran R, Colleran R, Angiolillo DJ, Byrne RA, Capodanno D, Cuisset T, Cutlip D, Eerdmans P, Eikelboom J, Farb A, Gibson CM, Gregson J, Haude M, James SK, Kim HS, Kimura T, Konishi A, Laschinger J, Leon MB, Magee PFA, Mitsutake Y, Mylotte D, Pocock S, Price MJ, Rao SV, Spitzer E, Stockbridge N, Valgimigli M, Varenne O, Windhoevel U, Yeh RW, Krucoff MW and Morice MC. Defining high bleeding risk in patients undergoing percutaneous coronary intervention: a consensus document from the Academic Research Consortium for High Bleeding Risk. Eur Heart J. 2019; 40: 2632-2653.
20)Levine GN, Jeong YH, Goto S, Anderson JL, Huo Y, Mega JL, Taubert K and Smith SC, Jr. Expert consensus document: World Heart Federation expert consensus statement on antiplatelet therapy in East Asian patients with ACS or undergoing PCI. Nat Rev Cardiol. 2014; 11: 597-606.
21)日本循環器学会 フォーカスアップデート版 冠動脈疾患患者における抗血栓療法 2020年.
22)Dewilde WJ, Oirbans T, Verheugt FW, Kelder JC, De Smet BJ, Herrman JP, Adriaenssens T, Vrolix M, Heestermans AA, Vis MM, Tijsen JG, van ‘t Hof AW, ten Berg JM and investigators Ws. Use of clopidogrel with or without aspirin in patients taking oral anticoagulant therapy and undergoing percutaneous coronary intervention: an open-label, randomised, controlled trial. Lancet. 2013; 381: 1107-15.
23)Committee CS. A randomised, blinded, trial of clopidogrel versus aspirin in patients at risk of ischaemic events (CAPRIE). CAPRIE Steering Committee. Lancet. 1996; 348: 1329-39.
24)Rollini F, Franchi F and Angiolillo DJ. Switching P2Y12-receptor inhibitors in patients with coronary artery disease. Nat Rev Cardiol. 2016; 13: 11-27.
25)Watanabe H, et al. STOPDAPT-2 ACS: One-month dual antiplatelet thrapy followed by clopidogrel monotherapy in acute coronary syndrome. ESC Congress 2021. https://www.escardio.org/The-ESC/Press-Office/Press-releases/Trial-does-not-support-clopidogrel-monotherapy-one-month-after-acute-coronary-syndromes
26)Patrono C. The Multifaceted Clinical Readouts of Platelet Inhibition by Low-Dose Aspirin. J Am Coll Cardiol. 2015; 66: 74-85.
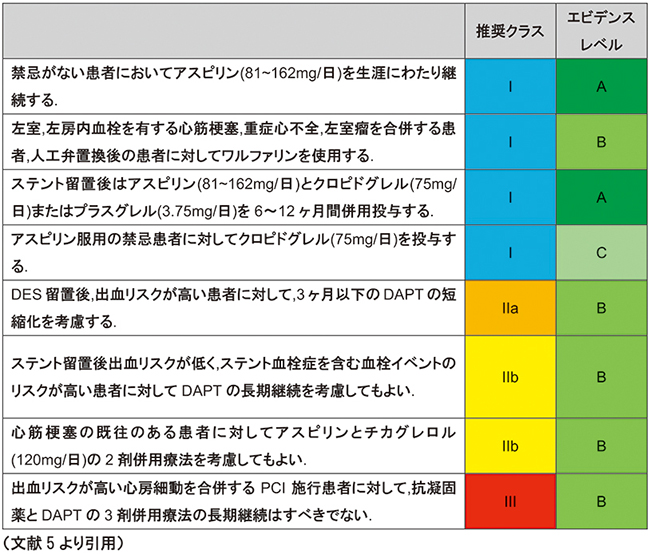
表1 2次予防における抗血栓薬投与に関する推奨とエビデンスレベル
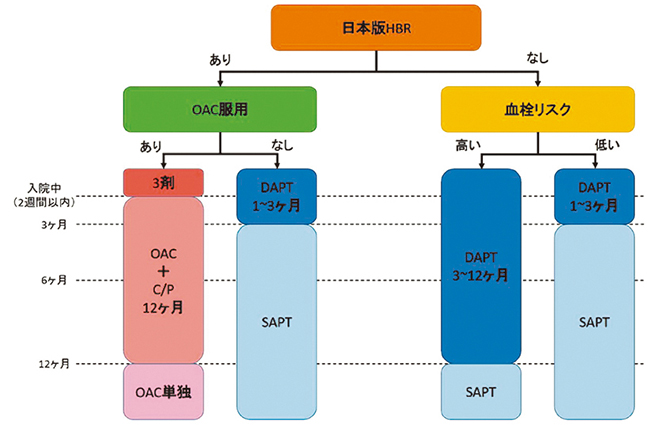
図 高出血リスク(HBR)をふまえたPCI施行後の抗血栓療法
注)短期間DAPTを選択した場合は、DAPT後のSAPTではP2Y12受容体拮抗薬を考慮する。OAC単独の場合には、投与可能であればDOACを推奨する。C/P:クロピドグレル/プラスグレル、DAPT:抗血小板薬2剤併用療法、HBR:高出血リスク、OAC:経口抗凝固薬SAPT:抗血小板薬単剤療法。(文献21より引用)
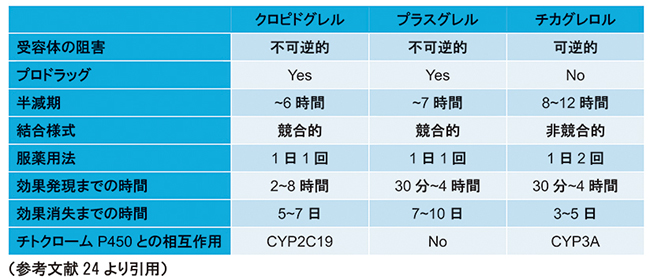
表2 P2Y12受容体拮抗薬の薬理作用の比較
(令和4年7月号)