新潟市医師会報より

NSAIDs治療の諸問題~酸分泌抑制薬による薬物療法~
新潟大学保健管理センター教授
黒田 毅
はじめに
非ステロイド性抗炎症薬(NSAIDs:Non-Steroidal Anti-Inflammatory Drugs)とは、抗炎症作用、鎮痛作用、解熱作用を有する薬剤の総称であり、局所におけるプロスタグランジンなどの活性物質の抑制によって作用を発揮する。臨床では、ほとんどすべての年齢層で用いられ、その適応は発熱を伴う疾患、疼痛を伴う疾患等、多岐にわたる。リウマチ性疾患では、関節リウマチ(Rheumatoid arthritis:RA)の関節痛や、膠原病の発熱、関節痛、頭痛、筋肉痛、皮膚や骨・軟骨の疼痛に使用される。
NSAIDsの作用機序
NSAIDsの作用機序はシクロオキシゲナーゼ(cyclooxygenase:COX)の阻害によるプロスタグランジン(prostaglandin:PG)やトロンボキサン(thromboxane:TX)などの産生の抑制である。COXには2つのアイソフォームが存在する。COX-1はすべての組織に常時発現しており、血管の恒常性、胃腸粘膜の血流や増殖、腎機能、血小板機能に関与している。COX-2は炎症性サイトカインの刺激を受けてマクロファージ、線維芽細胞、滑膜細胞などに発現誘導され、血管拡張作用などを有し炎症促進作用を持つ1)。またNSAIDsは、血中では大部分が血漿蛋白と結合した状態にあり主に肝臓において代謝される。そのため腎障害、肝障害、低アルブミン血症には注意が必要である。さらに肝臓おいては、同一酵素によって代謝される薬物が併用された場合、薬物の血中濃度が高まり、作用が強く現れる場合がある2)。
NSAIDsの種類
NSAIDsには経口剤、坐剤、貼付剤、塗布剤など様々な剤形がある。経口剤では半減期の長い1日1回投与のNSAIDsは、肝または腎機能が障害された患者や薬物代謝能が低下した高齢者において、血中濃度の上昇により副作用を合併しやすくなるため注意を要する。プロドラッグは体内で代謝されてはじめて活性体となる薬物である。胃腸障害が少ない特徴があるが、胃腸障害は完全には阻止できない3)。またNSAIDsの2剤以上の併用は副作用が増強し、効果の増強は望めないため行わない4)。坐剤は直腸粘膜を通して薬剤が吸収されるため、経口剤のような直接的な胃腸障害がなく速効性であるが、全身的副作用は経口剤と同様である。坐剤の使用において、高齢者では潜在的に腎機能障害が存在するため少量より開始することが重要である。湿布剤、塗布剤は経口剤や坐剤と比較して効果は弱いものの副作用は少ない。湿布剤の中には光線過敏症を起こすものがあるため貼付部位を確認して処方する。
NSAIDsの副作用
NSAIDsの主要な副作用を表1に示した。
1)NSAIDs潰瘍
NSAIDsは、COX-2を阻害することで、炎症に関与するPGの産生を抑制し、消炎・鎮痛効果を発揮するが一般的なNSAIDsでは、COX全体を阻害してしまうため、COX-2のみならず、胃粘膜保護などの役割をもつCOX-1も阻害してしまう。そのため、胃粘膜傷害が生じる原因となる。RA治療における消化管障害は重要な問題であった。RA患者において昭和40年から60年代までは上部消化管病変は、感染症、肺疾患に続く主要な死因の一つであった。本症の問題点は上部消化管症状の有無に関わらず消化性潰瘍が存在する点である。日本リウマチ財団が1991年に行ったNSAIDsによる上部消化管障害に関する疫学調査では全胃粘膜病変は全体の62.2%に認められ、胃潰瘍、十二指腸潰瘍はそれぞれ15.5%、1.9%であった5)。その後、昭和と平成年代を比較した和田らの報告において、H2ブロッカー、プロトンポンプ阻害薬(PPI)やこれに加えたミソプロストールの使用は、胃粘膜病変の防止に極めて有効であることが示された6)。
NSAIDs服用中は消化管出血を起こしても無症状の割合が多く好発部位は幽門部で次いで胃体部に好発する。一般的には小さく浅い潰瘍が多発し不正形のものが多いが前庭部の深い潰瘍や不正形の巨大潰瘍を形成する場合もある7)。セレコキシブなどのCOX-2選択的阻害薬の使用は非選択的阻害薬と比べて胃・十二指腸潰瘍などの粘膜障害を半減させる8)。また潰瘍発生率はNSAIDsの投与量に依存し用量が増加するほど発生率は増加し、多剤投与においても増加する9)。『消化性潰瘍診療ガイドライン2020改訂第3版』ではNSAIDs潰瘍の発症予防はボノプラザンを始めとするPPIによる予防が推奨されているものの、保険診療は潰瘍既往歴がある場合のみ認められ、潰瘍一次予防にPPIの使用は保険適応外である。潰瘍の既往がない場合のCOX-2選択的阻害薬の使用において潰瘍予防薬の併用は必要ないが、既往歴がある患者ではPPIによる潰瘍発生予防治療を行うことが推奨されている10)。NSAIDs潰瘍の高リスク因子としては、消化管出血を伴った潰瘍既往歴、中等度のリスク因子としては高齢者、潰瘍の既往、糖質ステロイドの併用、高用量NSAIDsや2種類以上のNSAIDs使用者、抗凝固・抗血小板作用のある薬剤の併用、Helicobacter pylori(H.pylori)陽性者、重篤な全身疾患を有する者、ビスホスホネートの併用が挙げられ、これらの因子が増えるほど、消化管出血のリスクが高くなるため高齢RA患者では特に注意が必要である11)。H.pyloriによる慢性胃炎、胃潰瘍や十二指腸潰瘍が報告されて以後、除菌が一般化してきているが、H.pyloriとNSAIDs潰瘍は互いに独立した因子であり、発生部位が異なる傾向が認められ、H.pylori除菌はNSAIDs潰瘍治療に影響を与えない12)。しかし、NSAIDs投与開始例でH.pyloriが陽性の場合には潰瘍予防として除菌が推奨されている13)。NSAIDs服用中は消化管出血を起こしても無症状の割合が多い。NSAIDs使用者には定期的な貧血のモニタリングと異常が認められた場合には内視鏡検査を行い早期にNSAIDs潰瘍の発症を確認する必要がある。
2)薬剤性腎障害
NSAIDsは薬剤性腎障害を起こす薬剤として認識されている。表2にNSAIDs腎障害の発症機序、病変の主座、臨床病型を示した。NSAIDsの腎障害は発生機序より①中毒性腎障害、②アレルギー機序による急性間質性腎炎、③薬剤による電解質異常、腎血流量減少などを介した間接毒性に分類される。NSAIDsで臨床的にしばしば遭遇するものとしては、急性腎障害を呈し、腎の尿細管、間質の障害により発症する尿細管間質障害型であり、血尿、タンパク尿などの尿異常、糸球体腎炎・ネフローゼ症候群等で発症する糸球体係蹄壁や糸球体構成細胞の障害による糸球体障害型は稀である。腎障害が既に存在している場合や高齢者、脱水等は危険因子となる。特に高齢者への夏場の使用は十分な服薬指導が重要である。腎機能の把握にはクレアチニン(Cr)の測定が一般的であるが、寝たきり患者を始めとして筋肉量の少ない場合の腎機能の把握にはシスタチンC(Cys-C)の有用性が注目されており、適宜利用しながら安全な投与を行う14)。
3)心血管系のイベントリスク
近年の報告では非選択的NSAIDs、および選択的COX-2阻害薬を含め、すべてのNSAIDsは心血管有害事象のリスクを上昇させるとされている15、16)。心血管有害事象は、短期使用、長期使用のいずれによっても生じているため、NSAIDsは最小有効用量を可能な限り最短期間使用することが望ましい。
4)肝障害
肝障害は軽度のトランスアミナーゼの上昇から劇症型の肝壊死まで種々の程度のNSAIDs関連肝障害がみられるが多くは可逆的である。重篤な肝障害をもつ患者ではNSAIDsの使用は控えるべきである17)。
5)その他の副作用
血液障害では貧血にしばしば遭遇するが貧血を認めた場合にはまず消化管出血や失血を考える。皮膚障害としては皮下出血、点状出血、紫斑が知られている。薬剤アレルギーで様々な皮疹が見られる。その他、イブプロフェンの無菌性髄膜炎、高齢者でのインドメタシンによる精神症状などが知られている。アスピリン喘息はCOX-1阻害作用をもつNSAIDsの投与により誘発される。成人喘息の約10%を占めると考えられているが、半数は潜在しておりNSAIDsを投与されることにより初めて顕在化する。アスピリン喘息の特徴として鼻炎、副鼻腔炎、鼻茸、嗅覚障害などの鼻・副鼻腔疾患の合併が多いため、使用前の病歴の聴取が重要である18)。
NSAIDsの注意すべき相互作用
実臨床で比較的多く遭遇する注意すべき相互作用を表3にまとめた。NSAIDsとニューキノロン系抗菌薬とを併用すると、けいれんを誘発することがある19)。NSAIDsは肝臓で代謝されるがCYP2C9で代謝されるため、ワルファリンの作用が増強され、出血傾向が発現する可能性がある。同様にフェニトイン、スルホニル尿素系血糖降下薬などと併用した場合もそれらの作用を増強する。尿細管分泌の競合により、リチウム、ジギタリス、メトトレキサートの排泄が遅延し、それらの作用を増強する。
NSAIDsの安全な使用法
高齢化を踏まえてNSAIDsを使用する場合の安全な使用法に関して以下の様に考える。NSAIDsを使用する際には他の医療機関で処方されている薬剤のチェック、場合により医療情報提供を行う。合併症リスクのチェックはまず消化器障害のリスクを考慮する。例として潰瘍の既往、高齢者、H.pyloriの有無、併用薬としてアスピリン、ワルファリン、ステロイドの有無などである。また喘息の有無も確認する。心血管系に関しては心筋梗塞、狭心症がある場合には多くは既に他の医療機関でフォローされている場合も多いためイベントリスクは把握しやすい。廃用症候群を始めとして筋肉量の少ない場合にはCrは低値となるため, Cys-Cを適宜追加し正確な腎機能の把握に努めるとともに、初回投与量は半量程度にすることも一つの考え方である。薬剤の選択は使用の状況が急性か慢性かを考慮する。急性の疼痛では半減期の短い短時間作用型、慢性疼痛においては中時間から長時間作用型が選択される。副作用の予防対策では消化管障害への対策が重要であり潰瘍既往歴、高齢者、ステロイドの併用者にはPPIやCOX-2選択的阻害薬であるセレコキシブの選択も予防対策となる。
おわりに
高齢者では腎機能、肝機能などは若年者と比べて低下しており、薬剤を安全に使用することが難しくなってくる。高齢化社会ではNSAIDsは骨関節疾患を始めとする多くの疾患に使用されるが、安全な使用が望まれる。
令和5年4月20日(木)
新潟市内科医会学術講演会にて講演
文献
1)佐野統.非ステロイド抗炎症薬(COX-2阻害薬).日本内科学会雑誌.2011;100:2888.
2)Bindua S, Mazumderb S, Bandyopadhyayb U. Non-steroidal anti-inflammatory drugs (NSAIDs) and organ damage: A current perspective. Biochem Pharmacol. 2020; 180: 114147.
3)齋藤輝信:関節リウマチにおけるNSAIDs と消化管病変.NSAIDsの使い方 ─コツと落とし穴.(水島裕・編),中山書店,東京,2006,pp.128-130.
4)Lanas A, García-Rodríguez LA, Arroyo MT, et al. Risk of upper gastrointestinal ulcer bleeding associated with selective cyclooxygenase-2 inhibitors, traditional non-aspirin non-steroidal anti-inflammatory drugs, aspirin and combinations. Gut 2006; 55: 1731.
5)塩川優一.非ステロイド性抗炎症剤による上部消化管傷害に関する疫学調査.リウマチ 1991;31:96-111.
6)和田庸子,村澤章,下条文武.RA患者に発生した胃粘膜病変 ─13年前との比較─.リウマチ科 2004;32:325-330.
7)Kim Y, Yokoyama S, Watari J, et al. Endoscopic and clinical features of gastric ulcers in Japanese patients with or without Helicobacter pylori infection who were using NSAIDs or low-dose aspirin. J Gastroenterol 2012; 47: 904-911.
8)Sakamoto C, Kawai T, Nakamura S, et al. Comparison of gastroduodenal ulcer incidence in healthy Japanese subjects taking celecoxib or loxoprofen evaluated by endoscopy: a placebo-controlled, double-blind 2-week study. Aliment Pharmacol Ther 2013; 37: 346-354.
9)Massó González EL, Patrignani P, Tacconelli S, et al. Variability among nonsteroidal anti-inflammatory drugs in risk of upper gastrointestinal bleeding. Arthritis Rheum 2010; 62: 1592-1601.
10)日本消化器病学会 消化性潰瘍診療ガイドライン2020(改訂第3版)東京:南江堂;2020.pp.116-131.
11)Masclee GM, Valkhoff VE, Coloma PM, et al. Risk of upper gastrointestinal bleeding from different drug combinations. Gastroenterology 2014; 147: 784-792.
12)Agrawal NM, Campbell DR, Safdi MA, et al. Superiority of lansoprazole vs ranitidine in healing nonsteroidal anti-inflammatory drug-associated gastric ulcers: results of a double-blind, randomized, multicenter study: NSAID-Associated Gastric Ulcer Study Group. Arch Intern Med 2000; 160: 1455-1461.
13)Tang CL, Ye F, Liu W, et al. Eradication of Helicobacter pylori infection reduces the incidence of peptic ulcer disease in patients using nonsteroidal anti-inflammatory drugs: a meta-analysis. Helicobacter 2012; 17: 286-296.
14)Sato H, Kazama J, Kuroda T, et al. Serum cystatin C measured by a sol particle homogeneous immunoassay can accurately detect early impairment of renal function. Clin Exp Nephrol. 2008; 12: 270.
15)Nissen SE, Yeomans ND, Solomon DH, et al. Cardiovascular safety of celecoxib, naproxen, or ibuprofen for arthritis. N Engl J Med. 2016; 375: 2519-2529.
16)MacDonald TM, Hawkey CJ, Ford I, et al. 2017. Randomized trial of switching from prescribed non-selective non-steroidal anti-inflammatory drugs to prescribed celecoxib: the Standard care vs. Celecoxib Outcome Trial (SCOT). Euro Heart J. 2017; 38: 1843-1850.
17)重篤副作用疾患別対応マニュアル 薬物性肝障害(肝細胞障害型薬物性肝障害、胆汁うっ滞型薬物性肝障害、混合型薬物性肝障害、急性肝不全、薬物起因の他の肝疾患)厚生労働省.2008;pp.30-33.
18)榊原博樹.アスピリン喘息.日内会誌.2009;98:3089-3095.
19)Kim J, Ohtani H, Tsujimoto M, et al. Quantitative comparison of the convulsive activity of combinations of twelve fluoroquinolones with five nonsteroidal antiinflammatory agents. Drug Metab Pharmacokinet. 2009; 24: 167-174.

表1 NSAIDsの副作用
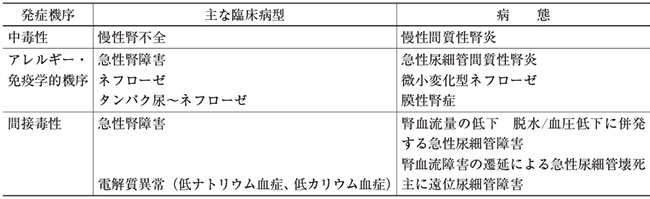
表2 発症機序によるNSAIDsによる薬剤性腎障害の主な臨床病型と病態
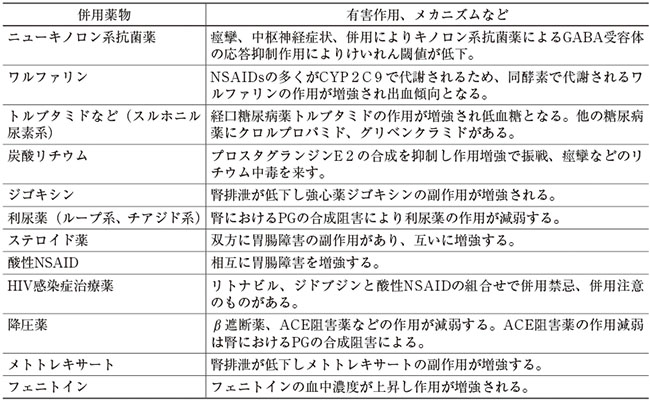
表3 NSAIDsの注意すべき相互作用
(令和5年12月号)